Un ensayo clínico aleatorizado con 318 pacientes en China demostró que ENDOVISTA-ENT, una herramienta de control de calidad en tiempo real, eleva la cobertura de sitios anatómicos del 83.5% al 93%, con beneficios especialmente pronunciados entre médicos con menos experiencia.
La nasofibrolaringoscopia el procedimiento endoscópico que permite examinar la cavidad nasal, la nasofaringe, la orofaringe, la laringe y la hipofaringe, es una herramienta central en el diagnóstico de enfermedades de la cabeza y el cuello, incluyendo cánceres de nasofaringe y laringe cuya tasa de supervivencia a cinco años supera el 90% cuando se detectan en etapa temprana. Sin embargo, la calidad del procedimiento depende en gran medida de la experiencia del especialista que lo realiza, lo que genera variabilidad en la exhaustividad de la exploración y puede traducirse en hallazgos perdidos. Un estudio publicado en npj Digital Medicine journal presenta la primera validación clínica prospectiva de un sistema de inteligencia artificial diseñado específicamente para monitorear la completitud de este procedimiento en tiempo real.
El sistema, denominado ENDOVISTA-ENT, fue desarrollado por investigadores del Hospital Universitario Ruijin de la Universidad Jiao Tong de Shanghái y el Primer Hospital Afiliado de la Universidad Sun Yat-sen en Guangzhou. A diferencia de la mayoría de las herramientas de AI endoscópica existentes, que se concentran en detectar lesiones en imágenes estáticas o fragmentos de video, ENDOVISTA-ENT no busca diagnosticar, sino verificar que el endoscopista haya visitado los sitios anatómicos clave durante la exploración. El sistema se conecta a través de la interfaz de video estándar de los endoscopios Olympus, sin modificar el equipo ni los pasos del procedimiento, y muestra en un monitor paralelo información sobre los sitios anatómicos ya cubiertos, el tiempo transcurrido y el progreso general del examen.
El desarrollo del modelo implicó el entrenamiento de dos clasificadores secuenciales sobre imágenes extraídas de videos de nasofibrolaringoscopia de 3,630 pacientes. El primero distingue entre imágenes dentro y fuera del cuerpo del paciente, con una precisión del 99.19%. El segundo identifica cuál de los once sitios anatómicos predefinidos aparece en cada fotograma, con una precisión del 98.40%. Ambos clasificadores utilizan la arquitectura EfficientNet-B0, que en las comparaciones realizadas mostró mejor desempeño que alternativas como ResNet50, ConvNeXt-Base y DenseNet121, con la ventaja adicional de requerir menor capacidad computacional. En condiciones de uso real, el sistema procesa los videos a 20 fotogramas por segundo, cumpliendo los requisitos de respuesta en tiempo real del entorno clínico.
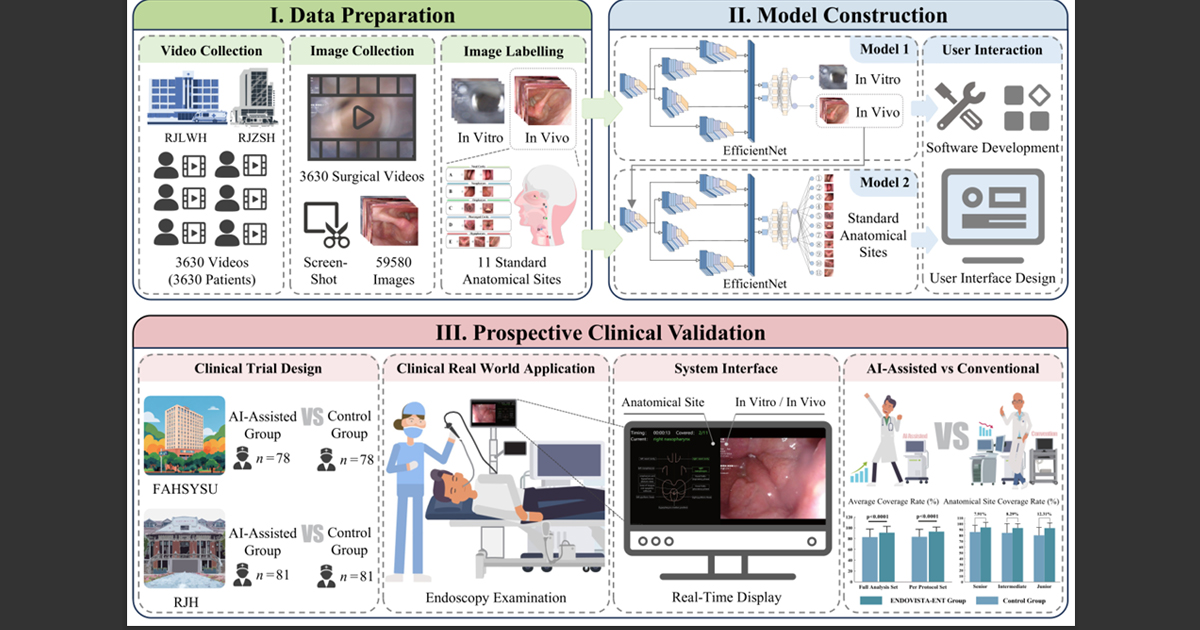
Para evaluar el impacto clínico del sistema, los investigadores diseñaron un ensayo controlado aleatorizado prospectivo, doble centro y simple ciego, realizado entre noviembre de 2024 y mayo de 2025 en los hospitales Ruijin y el Primer Hospital Afiliado de la Universidad Sun Yat-sen. Un total de 318 pacientes fueron asignados aleatoriamente en dos grupos iguales de 159 participantes, uno con asistencia de ENDOVISTA-ENT y otro con el procedimiento convencional, donde el monitor del sistema permanecía cubierto. Los resultados mostraron que el grupo asistido por AI alcanzó una cobertura media de sitios anatómicos del 93.08%, frente al 83.50% del grupo de control, una diferencia de 9.58 puntos porcentuales estadísticamente significativa. Crucialmente, esta mejora se logró sin aumentar de manera significativa el tiempo del procedimiento, que fue de 120.4 segundos en el grupo con AI frente a 113.0 segundos en el grupo de control.
El análisis por nivel de experiencia revela uno de los hallazgos más relevantes del estudio. El beneficio del sistema fue consistente en los tres grupos de endoscopistas, clasificados como junior, intermedio y senior, aunque el incremento más pronunciado se registró entre los médicos con menos experiencia, cuya cobertura pasó del 80.30% al 92.61%. El análisis estadístico de varianza confirmó que el efecto de la asistencia de AI fue significativo e independiente del nivel de experiencia del operador, sin que se observara interacción entre ambas variables. Esto sugiere que la herramienta puede servir tanto como apoyo en la práctica clínica habitual como instrumento de formación durante la curva de aprendizaje de médicos en entrenamiento.
Los autores señalan varias limitaciones. La cobertura anatómica, aunque es el indicador de calidad utilizado en el estudio, no garantiza por sí sola una visualización de calidad suficiente en regiones anatómicamente difíciles, donde la técnica del operador y las características individuales del paciente siguen siendo determinantes. El sistema fue evaluado exclusivamente con procesadores Olympus CV-170 y CV-190, por lo que su desempeño con otros equipos permanece sin validar. La imposibilidad de cegar a los endoscopistas respecto a su asignación de grupo constituye también una limitación inherente al diseño, aunque los investigadores mitigaron este efecto utilizando grabaciones en video y evaluación ciega de los resultados por un panel de expertos. Finalmente, el estudio no evalúa si una mayor cobertura anatómica se traduce efectivamente en tasas más altas de detección temprana de lesiones, una correlación que requerirá cohortes de validación más grandes con seguimiento prolongado.
Los investigadores plantean que el paradigma desarrollado, en el que la AI supervisa el proceso del procedimiento en lugar de intentar hacer diagnósticos, podría extenderse a otras especialidades que dependen de exploraciones endoscópicas o de imagen estandarizadas, como la gastroscopía, la colonoscopía, la broncoscopía o la ecografía, aunque advierten que cada campo requerirá definir sus propios indicadores de calidad y someterlos a validación específica.