Conoce más sobre la vacunación COVID-19

1. ¿Cuántas vacunas contra COVID-19 existen?
Las vacunas generalmente requieren años de investigación y pruebas antes de llegar al público, pero desde 2020 y ante la pandemia de COVID-19, científicos de todo el mundo están trabajando para producir vacunas seguras y efectivas contra el SARS-CoV-2 en un tiempo récord. Actualmente hay cientos de grupos de investigación desarrollando y probando vacunas de diversos tipos. Para el mes de enero de 2021, 66 vacunas se encuentran ya en ensayos clínicos en humanos, y 20 han llegado a las etapas finales de prueba.
Las vacunas más avanzadas ya han sido aprobadas para uso de emergencia por varios países. Entre éstas se encuentran:
- Abdala
- AstraZeneca/Oxford
- CanSinoBIO
- Covaxin
- Johnson & Johnson
- Moderna
- Novavax
- Pfizer/BioNTech*
- Sinopharm
- Sinovac
- Sputnik V
*El pasado 23 de agosto de 2021, la Administración de Medicamentos y Alimentos de los Estados Unidos (FDA, por sus siglas en inglés) otorgó aprobación total a la vacuna Pfizer/BioNTech para su uso en personas mayores de 16 años.
*El pasado 31 de enero de 2022, la FDA otorgó aprobación total a la vacuna Moderna para su uso en personas mayores de 18 años.
En México, las vacunas que han sido aprobadas por COFEPRIS (Comisión Federal para la Protección contra Riesgos Sanitarios) para uso por la emergencia sanitaria son:
- Abdala (29/12/2021)
- AstraZeneca/Oxford (04/01/2021)
- CanSinoBIO (08/02/2021)
- Covaxin (06/04/2021)
- Johnson & Johnson (27/05/2021)
- Moderna (17/08/21)
- *Pfizer/BioNTech (11/12/2020)
- Sinopharm (25/08/21)
- Sinovac (09/02/2021)
- Sputnik V (09/02/2021)
https://www.nytimes.com/interactive/2020/science/coronavirus-vaccine-tracker.html
https://www.gob.mx/cofepris/acciones-y-programas/vacunas-covid-19-autorizadas
* El pasado 3 de marzo de 2022, la COFEPRIS, autorizó la aplicación de la vacuna Pfizer/BioNTech para menores de 5 a 11 años
2. ¿Cuáles son los componentes de las vacunas contra COVID?
Cada vacuna tiene una formulación que consiste, en términos generales, en el antígeno o proteína del virus SARS-CoV-2 que será el encargado de provocar la respuesta inmune (mecanismo de defensa) del organismo y contra el cual se producen los anticuerpos y células activadas. Adicionalmente se incluyen sustancias necesarias para mantener la estabilidad del antígeno antes y después de la aplicación, así como para estimular la capacidad de respuesta del sistema inmunológico posterior a la aplicación de la vacuna.
A continuación, se describen los componentes de las cuatro vacunas actualmente disponibles para su aplicación:
La vacuna contra COVID-19 de Pfizer/BioNTech contiene los siguientes componentes:
- ARN (ácido ribonucleico) mensajero: el único componente activo de la vacuna. Las moléculas de ARNm contienen el material genético que proporciona instrucciones al organismo sobre cómo producir el antígeno: una proteína del virus llamada spike o espícula que desencadenará la respuesta inmune.
- Lípidos: su función principal es proteger la molécula de ARNm y proporcionar una cubierta exterior que ayuda a que el ARNm se introduzca en las células.
- Sales que permiten asegurar la estabilidad de la vacuna una vez inyectada en el organismo.
- Azúcar (sucrosa): Este componente ayuda a las moléculas a mantener su forma durante la congelación.
La vacuna contra COVID-19 de Moderna contiene:
- ARN (ácido ribonucleico) mensajero: al igual que la vacuna Pfizer BioNTech, también utiliza esta tecnología para generar anticuerpos contra COVID-19 que se encarga de desencadenar la respuesta inmune.
- Lípidos: para ayudar a transportar el ARNm a las células.
- Sustancias estabilizadoras como sales y sucrosa.
La vacuna de AstraZeneca/Oxford contiene:
- Un vector viral llamado Adenovirus ChAdOx1, el cual es un adenovirus de chimpancé, que no causa enfermedad en los humanos. Este virus lleva consigo el material genético (similar al ARNm de las vacunas de Pfizer y Moderna), el cual se encargará de producir la proteína espícula del SARS-CoV-2.
- Además del vector del material genético, la vacuna incluye sustancias para mantener su estabilidad.
La vacuna Sputnik V, desarrollada por el Centro Nacional Gamaleya, contiene:
- Dos vectores virales, Adenovirus 26 en la primera dosis y Adenovirus 5 en la segunda dosis. Ambos virus son debilitados para no causar enfermedad en las personas, pero capaces de llevar el material genético del virus, específicamente el gen que lleva las instrucciones para que las células humanas puedan producir la proteína espícula del SARS-CoV-2.
- Además del vector del material genético, la vacuna incluye sustancias para mantener su estabilidad.
La vacuna CanSinoBio contiene:
- Un vector viral, Adenovirus 5, el cual es un virus debilitado para no causar enfermedad en las personas, pero capaz de llevar el material genético del virus, específicamente el gen que lleva las instrucciones para que las células humanas puedan producir la proteína espícula del SARS-CoV-2.
- Además del vector del material genético, la vacuna incluye sustancias para mantener su estabilidad.
- Esta vacuna se aplica en una sola dosis.
La vacuna Johnson & Johnson contiene:
- Un vector viral, Adenovirus 26, el cual es un virus debilitado, al igual que en la vacuna CanSinoBio, para no causar enfermedad en las personas, capaz de llevar el material genético del virus, específicamente el gen que lleva las instrucciones para que las células humanas puedan producir la proteína espícula del SARS-CoV-2.
- Además del vector del material genético, la vacuna incluye sustancias para mantener su estabilidad.
- Esta vacuna se aplica en una sola dosis.
La vacuna Novavax contiene :
- Proteína Spike recombinante ensamblada en nanopartículas tridimensionales
- Un adyuvante
La vacuna Abdala contiene:
- Proteína S recombinante (dominio de unión con el receptor), clonada en una levadura y purificada.
- Hidróxido de aluminio como adyuvante
- Buffer de fosfatos.
Las vacunas contra COVID-19 Sinovac Biotech, Sinopharm y Covaxin, contienen el virus SARS-CoV-2 inactivado mediante una sustancia química llamada beta-propiolactona que quita al virus la posibilidad de reproducirse (replicarse) dentro de las células humanas, evitando que cause la enfermedad. Sin embargo, la proteína espiga o spike permanece intacta y con toda la capacidad para estimular la respuesta inmunológica del organismo para generar protección. Además del virus inactivado, la vacuna contiene una sustancia a base de aluminio llamada “adyuvante” que sirve para estimular aún más al sistema inmunológico para que responda adecuadamente a la vacuna.
Vacuna
País
Dosis
Componente
Eficacia
Autorizada en México
Pfizer / BioNTech
Estados Unidos / Alemania
2 dosis
ARN mensajero
95%
Autorizada en México
Moderna
Estados Unidos
2 dosis
ARN mensajero
94.5%
Autorizada en México
Abdala
Cuba
3 dosis
Proteína recombinante
92.5%
Autorizada en México
Sputnik V
Instituto de Investigaciones Gamaleya
Rusia
2 dosis
Adenovirus 26 Adenovirus 5
91%
Autorizada en México
COVAXIN
Instituto Nacional de Virología Bharat Biotech
India
2 dosis
Virus inactivado
81%
Autorizada en México
Sinopharm
Instituto de Productos Biológicos de Pekín
China
2 dosis
Virus inactivado
79%
Autorizada en México
AstraZeneca / Universidad de Oxford
Suecia - Inglaterra
2 dosis
Adenovirus ChAdOx1
76%
Autorizada en México
CanSinoBIO
Instituto de Biotecnología de Beijing
China
1 dosis
Adenovirus 5
64%
Autorizada en México
Johnson & Johnson
Estados Unidos
1 dosis
Adenovirus 26
67%
Autorizada en México
Sinovac
Sinovac Biotech
China
2 dosis
Virus inactivado
50.38%
Autorizada en México
Novavax
Estados Unidos
2 dosis
Proteína recombinante
90%
No autorizada en México
Moderna
País: Estados Unidos
Dosis: 2
Componente: ARN mensajero
Eficacia: 94.5%
Autorizada en México
Abdala
Cuba
3 dosis
Proteína recombinante
92.5%
Autorizada en México
Sputnik V
Instituto de Investigaciones Gamaleya
País: Rusia
Dosis: 2
Componente: Adenovirus 26 | Adenovirus 5
Eficacia: 91%
Autorizada en México
COVAXIN
Instituto Nacional de Virología Bharat Biotech
País: India
Dosis: 2
Componente: Virus inactivado
Eficacia: 81%
Autorizada en México
Sinopharm
Instituto de Productos Biológicos de Pekín
País: China
Dosis: 2
Componente: Virus inactivado
Eficacia: 79%
Autorizada en México
AstraZeneca / Universidad de Oxford
País: Suecia - Inglaterra
Dosis: 2
Componente: Adenovirus ChAdOx1
Eficacia: 76%
Autorizada en México
CanSinoBIO
Instituto de Biotecnología de Beijing
País: China
Dosis: 1
Componente: Adenovirus 5
Eficacia: 64%
Autorizada en México
Johnson & Johnson
País: Estados Unidos
Dosis: 1
Componente: Adenovirus 26
Eficacia: 67%
Autorizada en México
Sinovac
Sinovac Biotech
País: China
Dosis: 1
Componente: Virus inactivado
Eficacia: 50.38%
Autorizada en México
Novavax
País: Estados Unidos
Dosis: 2
Componente: Proteína recombinante
Eficacia: 90%
No autorizada en México

1. ¿Todas las vacunas funcionan igual?
Existen diversos tipos de vacunas actualmente desarrolladas o en desarrollo contra al SARS-CoV-2, el virus causante de COVID-19. A continuación se describen los principales mecanismos de acción de las vacunas:
- Ácidos nucleicos: Vacunas que transportan uno o más genes propios del coronavirus a las células humanas para producir proteínas virales que desencadenen la respuesta inmunitaria.
- Vectores virales: Vacunas que contienen virus diseñados para transportar genes de coronavirus. Las vacunas de vectores virales entran en las células y hacen que éstas produzcan proteínas virales que se expresan en la superficie de las células, para generar anticuerpos.
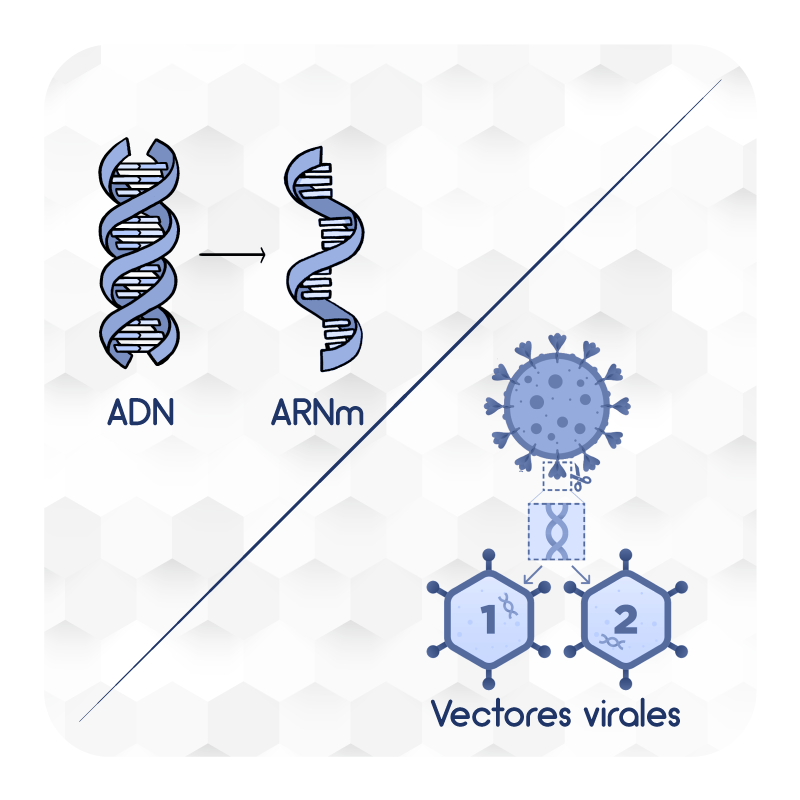
- Basadas en proteínas: Vacunas que contienen proteínas completas o fragmentos de proteínas de coronavirus, pero no material genético. Al detectar las proteínas virales, se desencadena la respuesta inmunitaria y se generan anticuerpos y células de defensa.
- Virus inactivados: Vacunas creadas a partir de coronavirus que han sido inactivados con productos químicos. Estos virus son capaces de desencadenar la respuesta inmune pero no de causar la enfermedad.
2. ¿Cómo funcionan las vacunas contra COVID?
Existen diversos tipos de vacunas actualmente desarrolladas o en desarrollo contra al SARS-CoV-2, el virus causante de COVID-19. Entre las vacunas disponibles se cuentan las siguientes:
Vacunas de ácidos nucleicos
Tanto las vacunas de Pfizer/BioNTech como la de Moderna, utilizan el ácido nucleico ARN mensajero (ARNm), una molécula con las instrucciones para la producción de proteínas por parte de las células. En el caso de estas vacunas, el ARNm tiene las instrucciones específicas para producir una proteína viral llamada proteína S, spike o espícula, la cual es esencial para que el virus infecte las células.
Después de la vacunación, las células reciben las instrucciones y comienzan a fabricar la proteína S y a exhibirla en su superficie. El sistema inmunológico identifica entonces la proteína viral y dispara la respuesta inmunológica produciendo anticuerpos y células de defensa.
https://www.mayoclinic.org/diseases-conditions/coronavirus/in-depth/coronavirus-vaccine/art-20484859
Vacunas de vectores virales
Para la vacuna de AstraZeneca, los investigadores agregaron el gen que produce la proteína S del coronavirus SARS-CoV-2 a otro virus llamado adenovirus. En este caso se utiliza una versión modificada de un adenovirus de chimpancé, conocido como ChAdOx1 que es inocuo para el ser humano. Este virus puede ingresar a las células, pero no puede replicarse dentro de ellas. Una vez dentro de la célula, el gen produce la proteína viral la cual se presenta en la superficie de la célula disparando la respuesta inmunitaria del organismo.
https://www.nytimes.com/interactive/2020/health/oxford-astrazeneca-covid-19-vaccine.html
Al igual que la vacuna de AstraZeneca, la vacuna del Centro Nacional Gamaleya de Investigación de Epidemiología y Microbiología de Rusia, Sputnik V, la vacuna de CanSinoBIO y la de Johnson & Johnson funcionan mediante un vector viral. La vacuna usa dos variantes de adenovirus, un tipo de virus que causa resfriados, al cual se le incluyó el gen con las instrucciones para producir la proteína espícula del coronavirus. Los dos tipos de adenovirus, Adenovirus 5 o Ad5 y Adenovirus 26 o Ad26 están diseñados para poder invadir las células para producir la proteína espícula, pero no son capaces de reproducirse ellos mismos. La estrategia de utilizar dos tipos de adenovirus busca evitar que la respuesta inmune del organismo impida que la segunda dosis de la vacuna funcione adecuadamente.
https://www.nytimes.com/interactive/2021/health/gamaleya-covid-19-vaccine.html
https://www.fda.gov/media/146305/download#page=2
Vacunas de virus inactivados
Las vacunas Sinovac Biotech, Sinopharm y Covaxin son vacunas de virus inactivado que utilizan la versión “muerta” del coronavirus que causa COVID-19.
Las vacunas inactivadas no suelen proporcionar una protección tan fuerte como las vacunas vivas. Es posible que se necesiten varias dosis a lo largo del tiempo (vacunas de refuerzo) para tener inmunidad continua contra la enfermedad.
Vacunas de proteínas recombinantes
La vacuna Novavax es la primera vacuna de proteína recombinante purificada y ensamblada en nanopartículas. Este tipo de vacunas son tecnológicamente diseñadas para ser muy estables, fáciles de transportar y de almacenar. No requieren red de frío a temperaturas ultrabajas, sino la red básica de 2-8 grados, lo cual las hace idóneas para su aplicación masiva.
3. ¿Todas las vacunas dan la misma protección?
No. De acuerdo con los experimentos e investigaciones publicados, después de la segunda dosis, o de la dosis única en su caso, la eficacia de las vacunas aprobadas es la siguiente:
- Pfizer/BioNTechtiene una eficacia de 95%
- Modernade 94.5%
- SputnikV de 91.4%
- Novavax 90.4%
- Covaxin de 81%
- Sinopharm de 79%
- AstraZeneca de 76%
- Johnson & Johnson (Janssen) de 67%
- CanSinoBio de 64%
- Sinovac de 50.38%
- Abdalác de 92%
https://www.nytimes.com/interactive/2020/science/coronavirus-vaccine-tracker.html
https://www.who.int/publications/i/item/WHO-2019-nCoV-vaccines-SAGE_recommendation-AZD1222-2021.1/
https://www.cdc.gov/coronavirus/2019-ncov/vaccines/different-vaccines/janssen.html
4. ¿Cómo sé que una vacuna es segura?
https://www.cdc.gov/coronavirus/2019-ncov/vaccines/safety.html
5. ¿Todas las vacunas son seguras?
Sí. Cada productor de vacuna publica los resultados de sus ensayos clínicos donde se presenta evidencia de la seguridad, eficacia, efectos adversos y contraindicaciones basados en los resultados de los experimentos realizados.
Esta información, junto con otros detalles de la vacuna como formulación y capacidad de generar protección es sometida a las autoridades regulatorias para solicitar la autorización de uso en cada país. La autorización de uso dependerá entonces de la evidencia de que una vacuna es segura y eficaz en proteger a la población contra la enfermedad.
En México, COFEPRIS ha otorgado ya la autorización para uso de emergencia a las vacunas de Pfizer/BioNTech, AstraZeneca, Sputnik V, Sinovac, CanSinoBIO, Covaxin, Johnson & Johnson, Moderna, Sinopharm y Abdala lo que significa que se permite la aplicación de estas vacunas únicamente como parte de la atención a la emergencia sanitaria por COVID-19.
https://www.bbc.com/mundo/noticias-55160530

1. ¿Todas las vacunas requieren de dos dosis?
Las vacunas de Pfizer, AstraZeneca, Moderna, Sputnik V, Sinovac y Sinopharm requieren de dos dosis. Las vacunas de CanSinoBIO y Johnson & Johnson requieren únicamente de una dosis.
Las vacunas contra el COVID-19 autorizadas en la actualidad requieren 2 dosis para que la protección sea máxima:
- Pfizer/BioNTech: las dosis se deben aplicar con un intervalo de 3 semanas (21 días)
- Moderna: las dosis se deben aplicar con un intervalo de 1 mes (28 días)
Debe darse la segunda dosis lo más cerca posible del intervalo recomendado de 3 semanas o 1 mes. Sin embargo, no existe un intervalo máximo entre la primera y la segunda dosis de ninguna de las dos vacunas. No debe darse la segunda dosis antes del intervalo recomendado.
- AstraZeneca/Oxford: Las dos dosis se deben aplicar con un intervalo de 28 días.
- Sputnik V: La segunda dosis se debe aplicar 21 días después de la primera.
- Sinovac: La segunda dosis debe aplicarse 2 semanas después de la primera.
- Covaxin: La segunda dosis se debe aplicar con un intervalo de 28 días.
- Sinopharm: la segunda dosis debe aplicarse 3 semanas después de la primera.
- Novavax: la segunda dosis se aplica un mes después de la primera.
- Abdala: la segunda dosis se aplica a los 14 días después de la primera y la tercera 14 días después de la segunda dosis.
https://www.nytimes.com/interactive/2021/health/gamaleya-covid-19-vaccine.html
https://www.nytimes.com/interactive/2020/science/coronavirus-vaccine-tracker.html
https://www.cdc.gov/coronavirus/2019-ncov/vaccines/faq.html
https://www.cdc.gov/coronavirus/2019-ncov/vaccines/different-vaccines/janssen.html
2. ¿Por qué es importante la aplicación de esquemas completos?
Uno de los elementos principales del proceso de desarrollo de las vacunas consiste en determinar el volumen y el número de dosis que las personas deben recibir para alcanzar el nivel de protección deseado contra la enfermedad. Esto determina finalmente el esquema de vacunación de cada vacuna, el cual es sometido a las autoridades regulatorias en cada país.
Por lo tanto, para lograr la protección contra la enfermedad, es importante cumplir con el número de dosis e intervalo entre cada uno establecido por el productor y autorizado por la autoridad regulatoria.
https://www.fda.gov/news-events/press-announcements/fda-statement-following-authorized-dosing-schedules-covid-19-vaccines
3. ¿Cuál es el tiempo máximo que tengo para aplicarme la segunda dosis de la vacuna?
Según los Centros para el Control de Enfermedades de Estados Unidos (CDC), el tiempo máximo para aplicarse la segunda dosis de cualquier vacuna es de 6 semanas posterior a la aplicación de la primera dosis.
- Pfizer/BioNTech: las dosis se deben aplicar con un intervalo de 3 semanas (21 días)
- Moderna: las dosis se deben aplicar con un intervalo 1 mes (28 días)
- AstraZeneca/Oxford: las dos dosis se deben aplicar con un intervalo de 1 mes (28 días)
- Sputnik V: La segunda dosis se debe aplicar a los 21 días de la primera
- Sinovac: Las dosis se deben aplicar con un intervalo de 2 semanas (14 días)
- Sinopharm: Las dosis se deben aplicar con un intervalo de 3 semanas (21 días)
- Covaxin: La segunda dosis se debe aplicar con un intervalo de 28 días.
- NOVAVAX: No hay información.
- Abdala No hay información
https://www.cdc.gov/vaccines/covid-19/info-by-product/clinical-considerations.html
https://www.cdc.gov/vaccines/covid-19/info-by-product/clinical-considerations.html
The Moderna COVID-19 (mRNA-1273) vaccine: what you need to know (who.int)
4. ¿Qué pasa si solo recibo una dosis?
No completar el esquema de vacunación recomendado puede ocasionar que no se alcance el nivel de protección inmunológica esperada contra la enfermedad. Esto es importante porque ante algunas variantes, como Delta, el efecto protector requiere forzosamente tener el esquema completo y haber transcurrido 14 días desde la última aplicación.
En este momento la evidencia científica apoya los esquemas definidos por los productores y autorizados por las agencias regulatorias como la COFEPRIS. Por ello, es importante que todas las personas que reciben sus vacunas contra COVID-19, tengan sus esquemas completos.
The Moderna COVID-19 (mRNA-1273) vaccine: what you need to know (who.int)
5. ¿Si me aplicaron la primera dosis con la vacuna de Pfizer, puedo aplicarme la segunda dosis con otra vacuna?
Hasta el momento hay evidencia científica que apoya la mezcla de algunos esquemas. Sin embargo, no existe una recomendación oficial al respecto en esta etapa de la estrategia de vacunación, ya que mezclar esquemas puede impactar en la disponibilidad de dosis suficientes para personas que no han recibido ninguna vacuna. Por lo tanto, la indicación actual es que ambas dosis del esquema deben completarse con el mismo producto.
https://www.cdc.gov/vaccines/covid-19/info-by-product/clinical-considerations.html
https://www.cdc.gov/vaccines/covid-19/info-by-product/clinical-considerations.html
The Moderna COVID-19 (mRNA-1273) vaccine: what you need to know (who.int)
https://www.who.int/publications/i/item/WHO-2019-nCoV-vaccines-SAGE_recommendation-AZD1222-2021.1/

1. Después de haber recibido la vacuna, ¿Al cuánto tiempo ya estoy protegido?
Para la vacuna de Pfizer, se alcanza niveles adecuados de protección contra la enfermedad, en el 95% de los vacunados, después de dos dosis, a los 28 días de haberse aplicado la primera dosis.
La vacuna Moderna alcanza niveles de protección adecuados del 94.5% a los 14 días después de la segunda dosis.
La protección de la vacuna de AstraZeneca, en su esquema óptimo, se da en el 76% de los vacunados después de dos dosis, entre dos y tres semanas tras la aplicación.
La vacuna Sputnik V, alcanza una efectividad del 73.1% a partir de la primera dosis y del 91.6% al aplicar la segunda dosis (día 21).
Para la vacuna CoronaVac de la empresa Sinovac, se alcanza una efectividad del 50.6% después de la aplicación de la segunda dosis, 14 días después de la primera.
La vacuna Johnson & Johnson, alcanza una efectividad del 67% a partir del día 14 de la aplicación de la única dosis.
La vacuna CanSinoBIO, alcanza una efectividad del 68.80% a partir del día 28 de la aplicación de la única dosis.
Actualmente, la vacuna Covaxin no tiene información disponible al respecto.
La vacuna Sinopharm alcanza su eficacia 14 días después de la segunda dosis.
La vacuna Novavax alcanza su eficacia 14 días después de la segunda dosis.
La vacuna Abdala alcanza su eficacia 14 días después de la tercera dosis.
https://www.thelancet.com/action/showPdf?pii=S0140-6736%2820%2932661-1
https://www.thelancet.com/action/showPdf?pii=S0140-6736%2821%2900234-8
https://www.thelancet.com/action/showPdf?pii=S0140-6736%2820%2931605-6
https://www.cdc.gov/coronavirus/2019-ncov/vaccines/different-vaccines/janssen.html
2. Si ya me vacuné, ¿Puedo dejar de usar cubrebocas y puedo dejar el aislamiento social?
No. Las vacunas no están diseñadas para bloquear la infección, sino para disminuir las hospitalizaciones y las defunciones. Por ello, es posible que personas vacunadas puedan infectarse, ya sea de manera sintomática o asintomática y así ser capaces de transmitir el virus a otras personas. Aunque hayas recibido tu esquema completo, se debe mantener el uso del cubrebocas para evitar la propagación del virus.
https://www.cdc.gov/coronavirus/2019-ncov/vaccines/faq.html
https://www.mayoclinic.org/diseases-conditions/coronavirus/in-depth/coronavirus-vaccine/art-20484859

1. ¿Puedo vacunarme contra el COVID al mismo tiempo que recibo otras vacunas?
Si bien la evidencia científica es limitada actualmente, no parece que las vacunas contra COVID-19 interfieran con la respuesta inmunitaria a otras vacunas y viceversa. Sin embargo, mientras no se tenga otra información, es recomendable esperar 14 días tras recibir la vacuna de COVID-19 para recibir otra vacuna. Del mismo modo, se deberá esperar 14 días para recibir la vacuna de COVID-19 tras haber recibido cualquier otra vacuna.
https://www.cdc.gov/coronavirus/2019-ncov/vaccines/faq.html
https://www.who.int/publications/i/item/WHO-2019-nCoV-vaccines-SAGE_recommendation-AZD1222-2021.1/

1. ¿Se puede aplicar la vacuna contra COVID en niños y adolescentes
Las aprobaciones de las autoridades regulatorias dependen de la evidencia de seguridad y eficacia presentada por los desarrolladores y productores de vacunas. En la actualidad, sólo una vacuna, Pfizer-BioNTech, ha sido autorizada para su aplicación en población de 12 a 17 años en presentación de 10 microgramos, y en niñas y niños de 5 a 11 años en presentación de 3 microgramos.
Actualmente, ya se han iniciado ensayos clínicos de varias vacunas en población entre 6 meses y 18 años de edad, por lo que se espera que hacia finales de 2021 se cuente con suficiente evidencia sobre la seguridad, la efectividad y los aspectos prácticos de la vacunación de esta población contra el coronavirus. Posteriormente se irán autorizando en poblaciones de menor edad, una vez que se tenga confianza en que la vacuna no causará ningún evento adverso grave en los niños.
https://www.thelancet.com/action/showPdf?pii=S0140-6736%2821%2900234-8


2. Si estoy embarazada, ¿Puedo aplicarme la vacuna?
Las vacunas son consideradas como uno de los productos médicos más seguros y con mayor beneficio para la salud de las personas. Por ello, las mujeres embarazadas y lactantes pueden optar por la aplicación de la vacuna ante un escenario de alto riesgo. Si tiene dudas sobre la vacunación en el embarazo, es recomendable consultar a un profesional de la salud.
https://www.cdc.gov/coronavirus/2019-ncov/vaccines/faq.html
https://www.who.int/publications/i/item/WHO-2019-nCoV-vaccines-SAGE_recommendation-AZD1222-2021.1/
3. Si estoy lactando, ¿Puedo aplicarme la vacuna?
Si bien no hay evidencia de que las vacunas contra COVID-19 puedan causar alteraciones a los bebés lactantes, aún no se tienen suficientes datos para apoyar la vacunación generalizada a las madres que estén amamantando a sus bebés. Sin embargo, las mujeres lactantes que formen parte de un grupo al que se recomienda recibir la vacuna COVID-19 (por ejemplo personal de salud con alto riesgo de exposición al virus o con comorbilidades) pueden optar por vacunarse. Si tiene dudas sobre la vacunación y la lactancia, es recomendable consultar a un profesional de la salud.
https://www.cdc.gov/coronavirus/2019-ncov/vaccines/faq.html
https://www.who.int/publications/i/item/WHO-2019-nCoV-vaccines-SAGE_recommendation-AZD1222-2021.1/
4. ¿Me puedo poner la vacuna de AstraZeneca/Universidad de Oxford aunque tenga más de 65 años?
La vacuna desarrollada por AstraZeneca/Universidad de Oxford puede ser utilizada por cualquier persona mayor de 18 años. Los resultados de los ensayos clínicos realizados demostraron que la vacuna es segura y eficaz en adultos mayores de 65 años. Es muy importante que este grupo de edad se vacune contra COVID-19 pues tiene un elevado riesgo de enfermedad grave o muerte por la enfermedad, situaciones que se previenen con la aplicación de la vacuna.
https://www.who.int/publications/i/item/WHO-2019-nCoV-vaccines-SAGE_recommendation-AZD1222-2021.1/
5. ¿Me puedo vacunar si soy una persona que vive con VIH?
De acuerdo con las recomendaciones para el uso de la vacuna de AstraZeneca/Universidad de Oxford publicadas por la Organización Mundial de la Salud, dado que esta vacuna no se puede reproducir en el organismo, sí puede ser administrada a personas que viven con VIH.
https://www.who.int/publications/i/item/WHO-2019-nCoV-vaccines-SAGE_recommendation-AZD1222-2021.1/
6. ¿Me puedo vacunar si soy una persona que padece de algún tipo de alteración de la inmunidad ya sea por tratamiento (por ejemplo inmunosupresores o quimioterapia) o enfermedad?
De acuerdo con las recomendaciones para el uso de la vacuna de AstraZeneca/Universidad de Oxford publicadas por la Organización Mundial de la Salud, dado que esta vacuna no se puede reproducir en el organismo, sí puede ser administrada a personas que padecen alguna alteración de la inmunidad, inmunodeficiencia o inmunosupresión.
https://www.who.int/publications/i/item/WHO-2019-nCoV-vaccines-SAGE_recommendation-AZD1222-2021.1/
7. ¿Me puedo vacunar si soy una persona que padece alguna enfermedad autoinmune (por ejemplo enfermedad celíaca, diabetes tipo 1, artritis reumatoide, lupus eritematoso, esclerosis múltiple)?
De acuerdo con las recomendaciones para el uso de la vacuna de AstraZeneca/Universidad de Oxford publicadas por la Organización Mundial de la Salud, dado que esta vacuna no se puede reproducir en el organismo, sí puede ser administrada a personas con padecimientos autoinmunes.
https://www.who.int/publications/i/item/WHO-2019-nCoV-vaccines-SAGE_recommendation-AZD1222-2021.1/

1. ¿Cuánto tiempo dura la protección de la vacuna?
No se sabe cuánto tiempo durará la inmunidad conferida por una vacuna COVID-19. Esto se debe a que se necesitan más datos de estudios en curso y adicionales a largo plazo para comprender cuánto tiempo dura la protección después de la vacunación.
2. ¿Tendremos que vacunarnos cada año?
Las autoridades de la Unión Europea coordinarán estudios independientes sobre el uso de las vacunas COVID-19 en la vida real, para recopilar más información sobre su seguridad y beneficio a largo plazo en la población en general. Los resultados de estos estudios a largo plazo conformarán las futuras estrategias de vacunación.

1. Si ya me dio COVID, ¿Puedo aplicarme la vacuna?
Las personas que ya han tenido COVID-19 o dieron positivo en la prueba pueden beneficiarse de la vacuna. Actualmente no hay suficiente información disponible para decir si las personas están protegidas contra el COVID-19 después de haberlo tenido (inmunidad natural) o durante cuánto tiempo. La evidencia preliminar sugiere que la inmunidad natural puede no durar mucho, pero se necesitan más estudios para comprender mejor esto.
Otras fuentes mencionan que debido a los riesgos graves para la salud asociados al COVID-19 y al hecho de que es posible la reinfección, es recomendable vacunarse. Si recibió tratamiento por síntomas del COVID-19 con anticuerpos monoclonales o plasma de convaleciente, debe esperar 90 días para aplicarse la vacuna correspondiente. Hable con su médico si no sabe con certeza qué tratamientos recibió, o si tiene más preguntas acerca de vacunarse contra el COVID-19.
https://www.cdc.gov/coronavirus/2019-ncov/vaccines/facts.html
De acuerdo con datos publicados por la Organización Mundial de la Salud, se considera que la reinfección por SARS-CoV-2 es rara en los primeros 6 meses posteriores a la infección sintomática. Por lo tanto, si bien las personas que han padecido COVID-19 pueden recibir la vacuna sin riesgo, se recomienda esperar 6 meses después de la enfermedad para recibir la primera dosis de la vacuna.
https://www.who.int/publications/i/item/WHO-2019-nCoV-vaccines-SAGE_recommendation-AZD1222-2021.1/
2. ¿Cuánto tiempo después de que me dio COVID puedo vacunarme?
Se debe posponer la aplicación de la vacuna en personas que recientemente han tenido COVID-19 y aún continúan con síntomas de este padecimiento. Por lo tanto, las personas con enfermedad confirmada por PCR y síntomas deben esperar a que desaparezcan los síntomas antes de recibir la primera dosis de la vacuna.
https://coronavirus.gob.mx/wp-content/uploads/2021/01/GuiaAplicacionVx_BNT162b_08Ene2021.pdf
https://www.who.int/publications/i/item/WHO-2019-nCoV-vaccines-SAGE_recommendation-AZD1222-2021.1/
3. ¿Qué dura más, la inmunidad después de haber tenido COVID o la protección de las vacunas contra COVID?
La protección que alguien obtiene al tener una infección (llamada “inmunidad natural”) varía según la enfermedad y varía de persona a persona. Debido a que este virus es nuevo, no sabemos cuánto tiempo podría durar la inmunidad natural. La evidencia actual sugiere que contraer el virus nuevamente (reinfección) es poco común en los 90 días posteriores a la primera infección con el virus que causa COVID-19.
No sabremos cuánto tiempo dura la inmunidad después de la vacunación hasta que tengamos más datos sobre qué tan bien funcionan las vacunas COVID-19 en condiciones del mundo real. Los expertos están trabajando para aprender más sobre la inmunidad natural y la inmunidad inducida por vacunas.

Los virus cambian constantemente a través de la mutación como parte de su evolución natural, y se espera que aparezcan nuevas variantes del virus con el paso del tiempo. A veces, emergen nuevas variantes y luego desaparecen. En otras ocasiones, emergen nuevas variantes y persisten. Se han documentado diversas variantes del virus que causa el COVID-19 a nivel mundial durante esta pandemia.
El virus que causa el COVID-19 es un tipo de coronavirus, una gran familia de virus. Los coronavirus reciben este nombre debido a los picos en forma de corona que se encuentran en su superficie. Estos picos son las estructuras mediante las cuales el coronavirus causante de COVID-19 se une a las células para infectarlas. Los científicos monitorean los cambios del virus, incluidos los cambios en los picos de la superficie. Estos estudios, que incluyen análisis genéticos del virus, ayudan a los científicos a entender cómo los cambios en el virus pueden incidir en la forma en que se propaga y lo que le pasa a las personas que se infectan con él.
Hay diferentes variantes del virus que causa el COVID-19 en circulación en el mundo, las más importantes son las siguientes:
- El Reino Unido (RU) identificó una variante llamada Alfa con una gran cantidad de mutaciones en el otoño del 2020.
Esta variante se propaga con mayor facilidad y rapidez que las otras variantes. En enero de 2021, los expertos del RU informaron que esta variante puede estar asociada a un mayor riesgo de muerte, en relación con las otras variantes del virus, pero es necesario seguir investigando para confirmar este hallazgo. Desde entonces, se ha detectado en muchos países del mundo. El primer caso de esta variante en los Estados Unidos fue detectado a fines de diciembre de 2020.
- En Sudáfrica apareció otra variante llamada Beta, detectada en octubre de 2020, y comparte algunas mutaciones con la variante Alfa. A fines de enero del 2021 también se notificaron casos causados por esta variante en los Estados Unidos.
- En Brasil apareció una variante llamada Gamma, que se identificó por primera vez en viajeros provenientes de Brasil sometidos a las pruebas de detección de rutina en un aeropuerto de Japón a principios de enero. Esta variante contiene un juego de mutaciones adicionales que podrían afectar su capacidad de ser reconocida por los anticuerpos. El primer caso de esta variante en los Estados Unidos fue detectado a fines de enero de 2021.
- En India, en febrero de 2021 se identificó la variante denominada Delta, la cual es la más transmisible de todas las variantes conocidas y actualmente es la variante dominante en el mundo. Esta variante presenta además cierta capacidad de evasión inmune, por lo que ha impactado en la eficacia de todas las vacunas actualmente disponibles, no obstante, este impacto es menor en las personas que tienen esquemas completos de vacunación y que tienen más de 14 días de haberlo completado.
- La variante Ómicron se identificó en Sudáfrica en noviembre de 2021. Tiene 3 veces más mutaciones en la proteína de espícula en comparación con la variante Delta. Rápidamente se dispersó en todos la mayoría de los continentes y sus mutaciones se han asociado a evasión inmune, tanto en vacunados, como en personas infectadas previamente.

Estas variantes parecen propagarse con mayor facilidad y rapidez que las otras variantes, lo que podría generar más casos de COVID-19.
Hasta el momento, los estudios sugieren que los anticuerpos generados a través de la vacunación, con las vacunas autorizadas en la actualidad, reconocen estas variantes. Este aspecto se está estudiando atentamente y hay más investigaciones en curso.
https://espanol.cdc.gov/coronavirus/2019-ncov/transmission/variant.html















