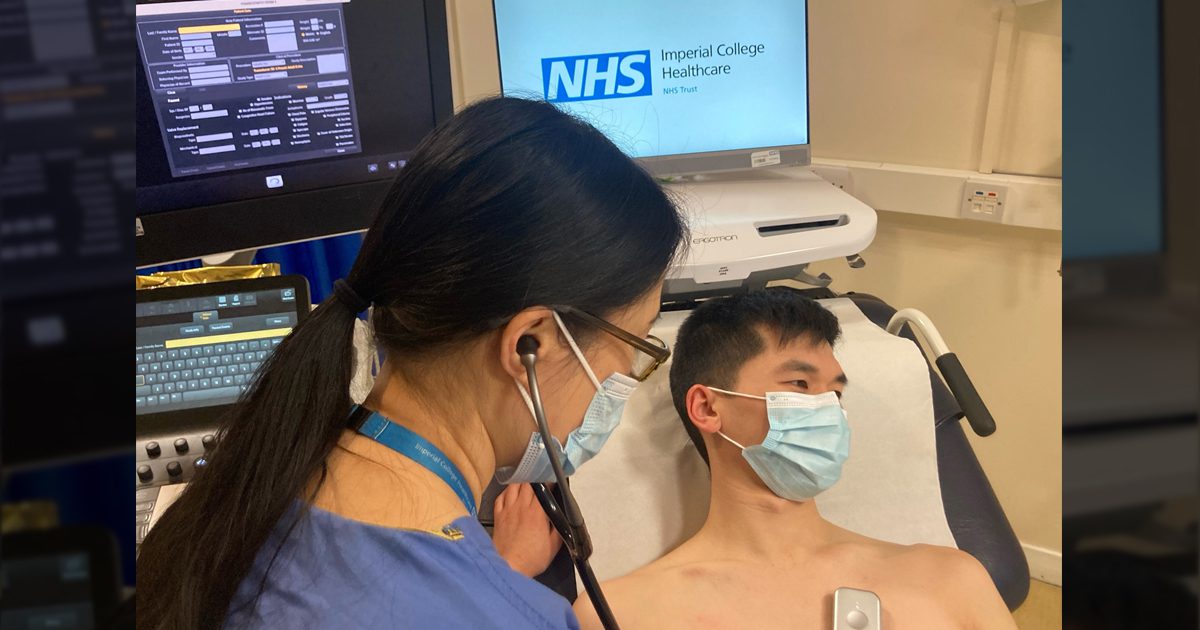
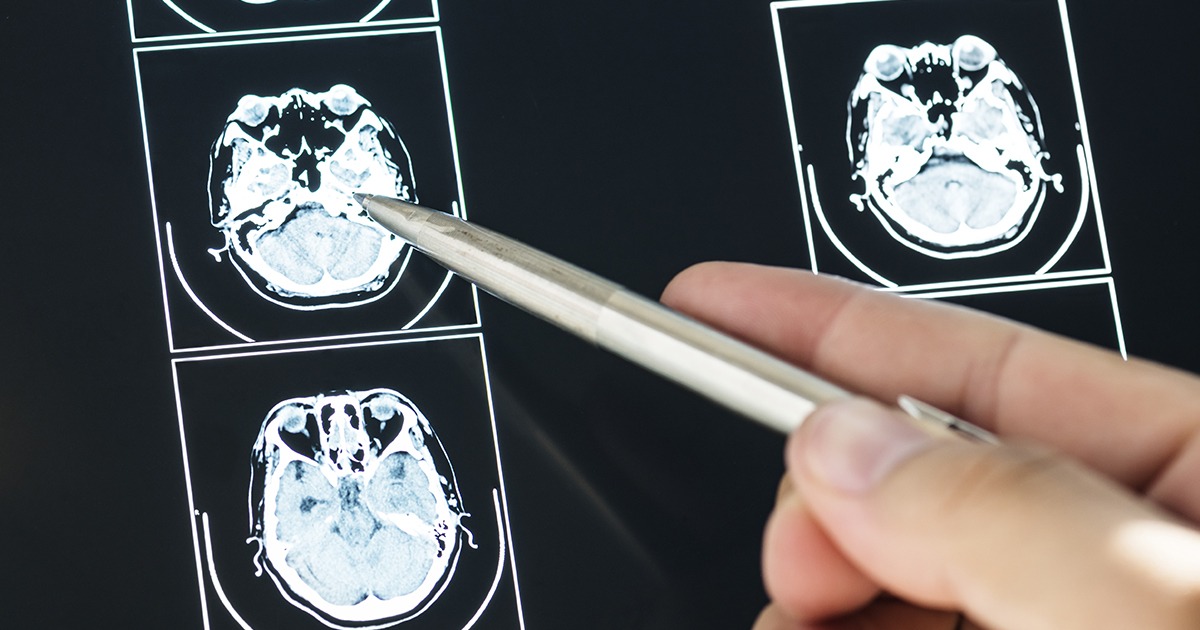
Las compañías farmacéuticas y las organizaciones de investigación utilizan los ensayos clínicos para probar y evaluar la eficacia y seguridad de tratamientos, medicamentos o terapias médicas.
Los ensayos clínicos son fundamentales para el avance de la medicina y para garantizar que los tratamientos sean seguros y eficaces antes de su aprobación y uso generalizado. La pandemia por COVID-19 impulsó la implementación y adopción de los ensayos clínicos descentralizados (DCT), tal y como ocurrió con otras soluciones de Salud Digital como el monitoreo remoto de pacientes, la telemedicina o el registro de síntomas. Los nuevos ensayos clínicos se han adaptado a la descentralización de elementos un cambio que ha involucrado diversos enfoques y métodos de monitoreo o asistencia remota.
Los ensayos clínicos descentralizados permiten la utilización de diversas herramientas digitales que facilitan la investigación sin necesidad de contacto físico entre los equipos de investigación y los participantes. Especialmente en etapas como el reclutamiento, la inscripción, el consentimiento informado y la administración de las intervenciones.
En este sentido, los ensayos clínicos convencionales requieren que los investigadores y los participantes se encuentren en un mismo sitio para recibir indicaciones sobre cómo va a funcionar la investigación. Es decir, que reúnen a los participantes en centros de salud académicos, en días y horarios establecidos para realizar las tareas de investigación.
Por otra parte, los ensayos clínicos descentralizados permiten la participación, consecución de tareas y recopilación de datos de manera remota. De esta manera, ofrecen mejoras en la recepción de datos en tiempo real y cuidan la privacidad y seguridad de los mismos. Gracias a herramientas como la telemedicina y el uso de dispositivos móviles es posible llevar a cabo este tipo de ensayos, acelerando los procesos de investigación y reduciendo costos.

Debido al auge de este tipo de ensayos durante la pandemia la Administración de Drogas y Alimentos de Estados Unidos (FDA, en inglés) hizo énfasis sobre la importancia de evaluar tanto los riesgos como los beneficios de los ensayos clínicos descentralizados. Asimismo, organismos de diversos países han implementado guías regulatorias para este tipo de ensayos, a través de agencias similares a la FDA. Por ejemplo, la Comisión Europea los regula a través de la Agencia Europea de Medicamentos; Canadá a través de Health Canadá; o Australia a través del Departamento de Salud; entre otros.
Un análisis publicado en The Lancet Digital Health, propone algunas consideraciones éticas para los ensayos clínicos descentralizados:
Mejorar la seguridad de los participantes y proteger sus derechos
Promover la seguridad de los participantes y proteger sus derechos incluye la consideración de la seguridad física, la privacidad, el consentimiento informado y el bienestar. Para ello contemplan la seguridad física, la privacidad en el uso de herramientas digitales, el consentimiento informado y el bienestar de los participantes.
Garantizar la validez científica
El valor científico de un ensayo clínico es una condición previa para justificar la inscripción de participantes. Es decir que no se debe elegir un enfoque descentralizado únicamente porque es más conveniente o menos costoso que un estudio presencial, según explican los autores.
Supervisión ética mejorada
Al igual que en el punto anterior, los autores consideran que la descentralización no debe ser la única vía para los ensayos clínicos. “Los investigadores y los comités de ética de la investigación deberán aumentar su vigilancia al identificar los nuevos riesgos que surgen en los DCT. A pesar de la promesa de los ensayos clínicos descentralizados de abordar muchas de las deficiencias de los ensayos clínicos convencionales, no todos los ensayos serán adecuados para este enfoque. Por lo tanto, la elección de la descentralización requiere una cuidadosa consideración”, indican los autores.
Conoce más sobre los ensayos clínicos descentralizados y sus condiciones éticas https://www.thelancet.com/journals/landig/article/PIIS2589-7500(23)00052-3/fulltext