Un índice metabólico basado en muestras de sangre seca y aprendizaje profundo o deep learning mejora la estratificación del riesgo neonatal
Un estudio liderado por Stanford Medicine y publicado en Science Translational Medicine presenta una nueva herramienta basada en inteligencia artificial que permite predecir el riesgo de complicaciones graves en bebés prematuros a partir de muestras de sangre recolectadas poco después del nacimiento. El enfoque utiliza perfiles metabólicos obtenidos de las pruebas de tamizaje neonatal rutinarias y modelos de deep learning or deep learning para ofrecer una evaluación más precisa del estado de salud de los recién nacidos que los métodos clínicos tradicionales.
La prematuridad neonatal está asociada con una alta morbilidad y mortalidad, en gran parte debido a complicaciones adquiridas como la displasia broncopulmonar, la hemorragia intraventricular, la enterocolitis necrotizante y la retinopatía del prematuro. Sin embargo, las clasificaciones actuales basadas en la edad gestacional y el peso al nacer no logran explicar por completo por qué bebés con características similares pueden tener trayectorias clínicas muy distintas. Ante esta limitación, el equipo de investigación planteó que los perfiles metabólicos capturan información biológica adicional relevante para estratificar el riesgo desde las primeras horas de vida.
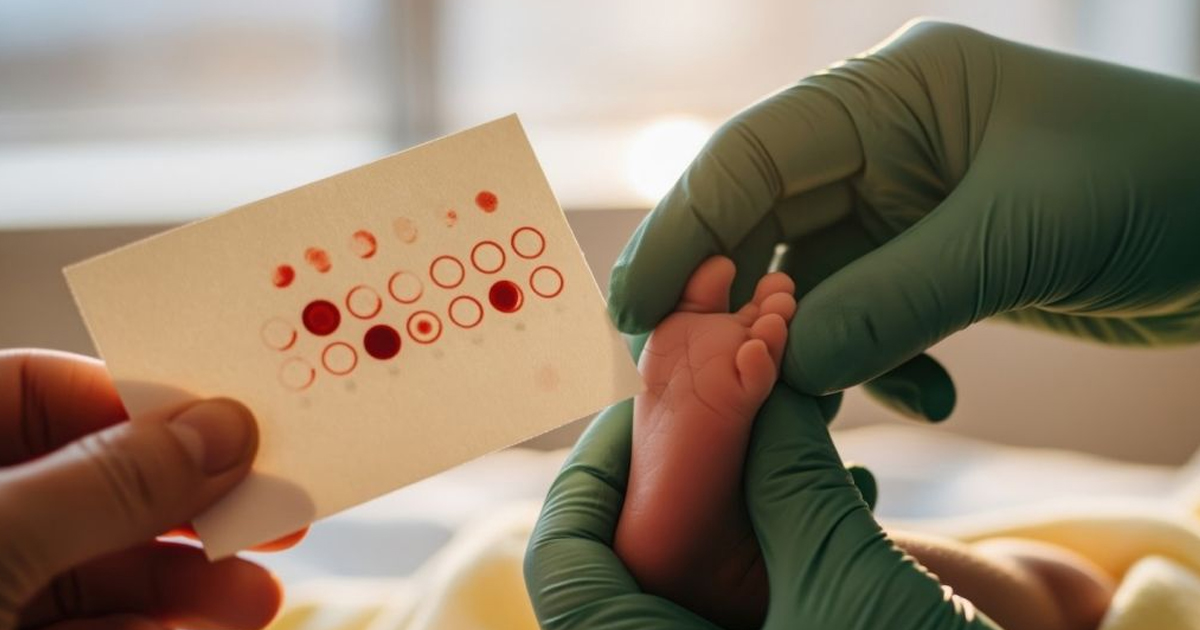
El estudio analizó 13,536 muestras de sangre seca de recién nacidos prematuros en California, recolectadas dentro de las primeras 48 horas tras el nacimiento y vinculadas con datos clínicos de seguimiento. A partir de esta información, los investigadores desarrollaron un índice metabólico de salud neonatal mediante un modelo de deep learning, capaz de identificar el riesgo de desarrollar una o más de las principales complicaciones de la prematuridad. Este índice demostró un desempeño superior al de otros algoritmos de machine learning y a los modelos basados únicamente en factores clínicos.
“El nacimiento prematuro no es un solo problema, sino varios problemas distintos”, explicó Nima Aghaeepour, coautor senior del estudio. “No podemos simplemente meter a todos los bebés nacidos antes de tiempo en una sola categoría de ‘prematuros’”. Según el investigador, el uso de mediciones biológicas obtenidas al nacer permitió “crear una nueva definición de la prematuridad basada en los resultados reales de estos bebés”.
The modelo fue validado de manera externa en una cohorte independiente de 3,299 recién nacidos muy prematuros en Ontario, Canadá, donde replicó los principales subgrupos metabólicos de riesgo identificados en la cohorte original. Los resultados respaldan la posibilidad de que este índice metabólico funcione como una métrica biológica generalizable de la prematuridad, dado que el tamizaje neonatal mediante muestras de sangre seca es una práctica extendida en muchos países.
The análisis identificó patrones específicos en moléculas relacionadas con el metabolismo, como aminoácidos y productos del metabolismo de grasas, que se asociaron con la aparición posterior de complicaciones. Con base en estas señales, los investigadores definieron un conjunto reducido de mediciones metabólicas que conforman el núcleo del índice, el cual se complementa con variables clínicas básicas. En conjunto, el modelo logró predecir el desarrollo de cada una de las cuatro complicaciones principales con una precisión superior al 85%.
“El objetivo es tener una nueva taxonomía de la prematuridad, que permita ver hacia dónde se dirige un niño y entender qué está causando las diferencias en sus trayectorias de salud”, señaló David Stevenson, coautor del estudio. “Eso nos permitirá intervenir, prevenir y tratar las complicaciones”.
Además de su potencial predictivo, el enfoque abre nuevas vías para comprender la biología subyacente de la prematuridad. “Antes no sabíamos qué había ‘bajo el cofre’, por así decirlo”, afirmó Stevenson. “Ahora estamos observando directamente la maquinaria biológica y cómo está funcionando”.
El equipo de investigación planea ampliar el modelo incorporando información adicional, como datos del embarazo materno, registros clínicos electrónicos y otros marcadores biológicos. A largo plazo, los autores señalan que esta herramienta podría ayudar a orientar decisiones clínicas tempranas, como el nivel de atención neonatal requerido o la comunicación del pronóstico a las familias. “La oportunidad de crear valor para la sociedad es verdaderamente extraordinaria”, concluyó Aghaeepour. “Cada bebé prematuro que salvamos representa toda una vida de años saludables”.







