Una revisión analiza cómo la IA está transformando la detección, caracterización y seguimiento del cáncer de próstata a través de ultrasonido, resonancia magnética y PET/TC.
El cáncer de próstata es una de las principales causas de muerte por cáncer en hombres a nivel mundial. De acuerdo con datos de GLOBOCAN 2022, cada año se diagnostican más de 1.4 millones de casos y se registran alrededor de 370 mil muertes. La supervivencia a cinco años puede alcanzar 99% cuando el tumor se detecta en etapas localizadas, pero cae por debajo de 30% en enfermedad metastásica. En este contexto, el diagnóstico temprano y la adecuada estratificación del riesgo son determinantes para definir tratamientos personalizados y reducir la mortalidad.
Una revisión publicada en npj Digital Medicine examina el papel actual y las perspectivas futuras de la inteligencia artificial (IA) en la imagen diagnóstica del cáncer de próstata. El artículo integra evidencia sobre ultrasonido transrectal, resonancia magnética multiparamétrica y la tomografía por emisión de positrones (PET)/tomografía computarizada (TC) o PET/TC, con trazadores dirigidos al antígeno de membrana prostática específica, además de abordar retos técnicos, clínicos y éticos para su implementación.
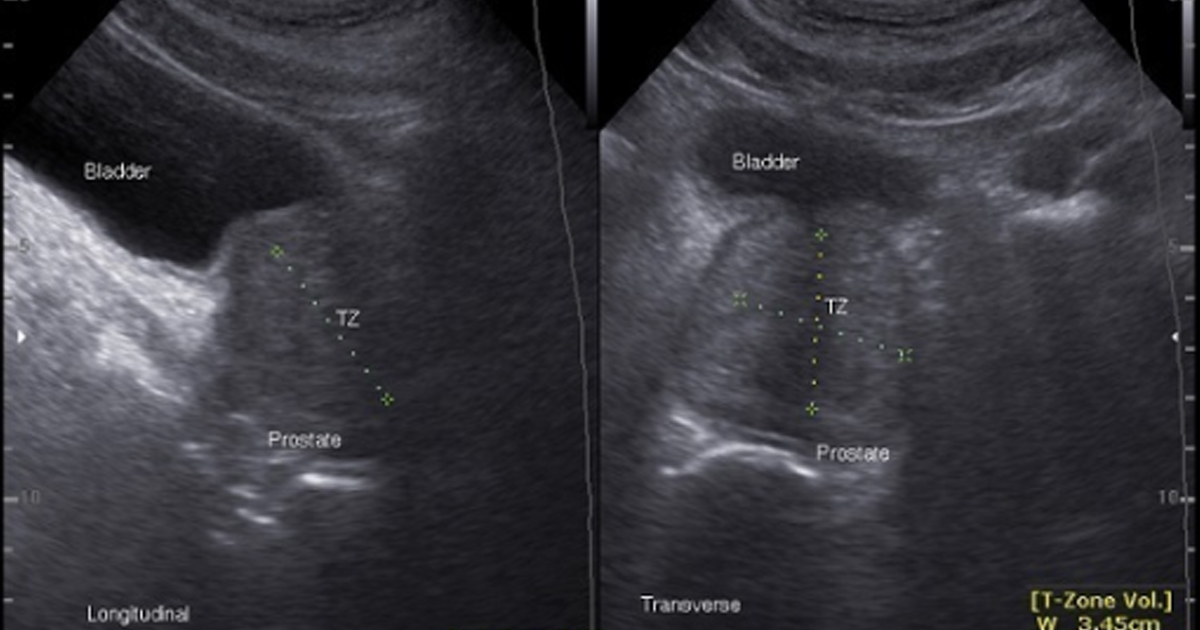
En el caso del ultrasonido, técnica ampliamente utilizada por su bajo costo y disponibilidad, la especificidad tradicional es limitada debido a la superposición entre lesiones malignas e hiperplasia benigna o prostatitis. Los modelos de aprendizaje automático o machine learning y aprendizaje profundo o deep learning han permitido mejorar la detección de lesiones sospechosas mediante redes convolucionales que identifican regiones de interés en tiempo real y reducen la dependencia del operador. Algunos sistemas han alcanzado sensibilidades superiores a 90% y han mostrado capacidad para disminuir biopsias innecesarias, especialmente en pacientes con niveles de PSA en la llamada zona gris.
La radiómica basada en ultrasonido también ha demostrado utilidad para diferenciar tejido benigno y maligno mediante la extracción de características cuantitativas de textura e intensidad. En estudios con cientos de pacientes, modelos como bosques aleatorios o máquinas de soporte vectorial han superado el desempeño del ultrasonido convencional y del PSA sérico en términos de área bajo la curva, lo que sugiere un potencial importante como herramienta complementaria en la toma de decisiones clínicas.
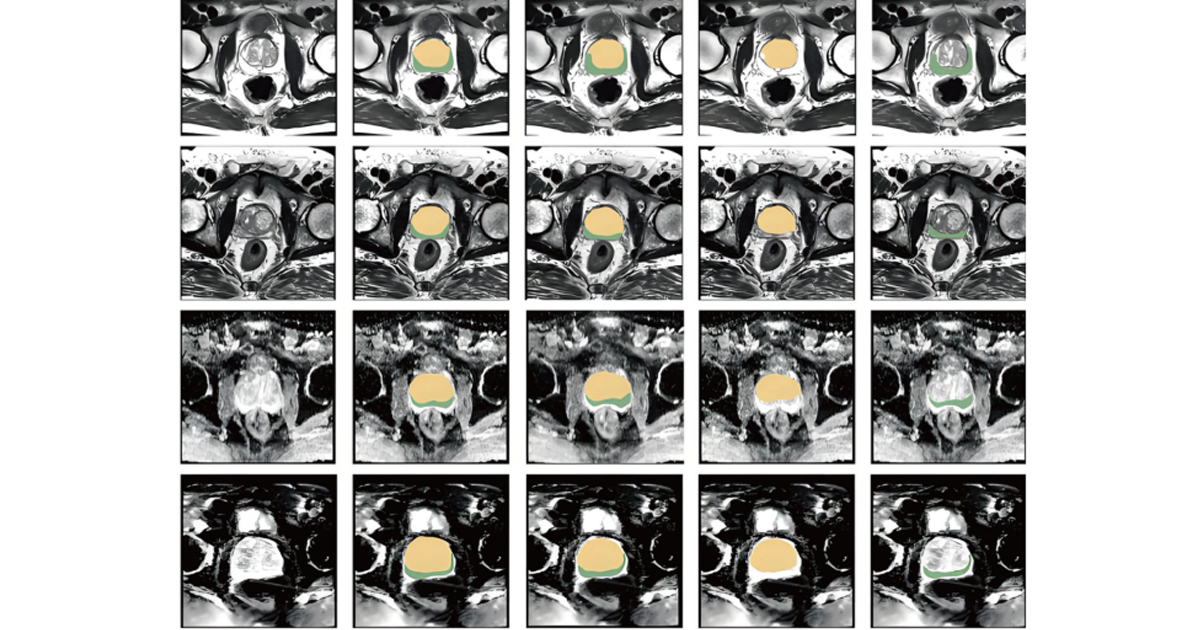
En resonancia magnética multiparamétrica, considerada el estándar de referencia para detectar cáncer de próstata clínicamente significativo, la IA ha avanzado en tres frentes principales, la segmentación automática de la glándula y sus zonas anatómicas, la identificación precisa de tumores relevantes y la predicción de parámetros pronósticos. Los algoritmos de segmentación basados en arquitecturas como U-Net han reducido el tiempo de delineación de estructuras y han mejorado la consistencia entre centros. A su vez, modelos de fusión multisecuencia, incluidos enfoques basados en Transformers, han mostrado un desempeño comparable o incluso superior al de radiólogos experimentados en la detección de tumores pequeños, además de disminuir la variabilidad interobservador.
En la evaluación dinámica con resonancia contrastada, redes neuronales recurrentes han logrado analizar automáticamente curvas de perfusión tumoral y estimar parámetros asociados con angiogénesis, algunos de los cuales se correlacionan con el puntaje de Gleason y con el riesgo de recurrencia bioquímica. Esto abre la puerta a utilizar biomarcadores derivados de imagen como indicadores pronósticos no invasivos.
La PET/TC con trazadores dirigidos a Antígeno Prostático Específico de Membrana (PSMA, en inglés) desempeña un papel clave en la detección de metástasis y en el seguimiento terapéutico. Aquí, los modelos de aprendizaje profundo han sido capaces de segmentar lesiones óseas y ganglionares de forma automática, cuantificar la carga tumoral total y mejorar la sensibilidad frente a la interpretación convencional. Además, enfoques basados en aprendizaje contrastivo han permitido predecir de manera temprana la respuesta al tratamiento sistémico, facilitando ajustes oportunos en la estrategia terapéutica.
La revisión destaca resultados de estudios clínicos en escenarios cercanos a la práctica real. En evaluaciones multicéntricas con miles de estudios de resonancia, los sistemas de IA han mostrado sensibilidad no inferior a la de radiólogos promedio y especificidad comparable a decisiones multidisciplinarias estándar. También se ha observado que la asistencia con IA puede aumentar la sensibilidad de lectores menos experimentados, reducir tiempos de lectura y mejorar la concordancia entre profesionales.
Entre los obstáculos encontrados por los autores destacan la disponibilidad de bases de datos amplias y diversas, pues estas son limitadas y predominan solo en hospitales de alta especialidad y hay poca representación en centros de atención primaria y poblaciones diversas. Las diferencias en equipos y protocolos generan problemas de generalización, conocidos como cambios de dominio, que reducen el desempeño cuando los modelos se aplican en entornos distintos a aquellos en los que fueron entrenados. Además, la sensibilidad a artefactos de imagen y la escasa representación de subtipos raros pueden afectar la robustez diagnóstica.
En el plano clínico, la falta de explicabilidad de muchos modelos, percibidos como cajas negras, limita la confianza de los médicos. Encuestas citadas en la revisión muestran que la adopción aumenta significativamente cuando las decisiones de la IA coinciden con la experiencia del profesional, lo que pone en evidencia la necesidad de sistemas interpretables que integren mapas de calor, justificaciones basadas en características relevantes y reportes estructurados alineados con los flujos de trabajo hospitalarios.
De cara al futuro, los autores proponen cuatro líneas estratégicas: La primera es la construcción de consorcios multicéntricos y el uso de aprendizaje federado para entrenar modelos sin necesidad de compartir datos sensibles, preservando la privacidad. La segunda es el desarrollo de técnicas de adaptación de dominio y entrenamiento robusto frente a artefactos. La tercera es el diseño de modelos específicos para distintos escenarios clínicos, como tamizaje ambulatorio, planificación de biopsias o vigilancia postratamiento. La cuarta es la integración de datos multiómicos, combinando radiómica con información genómica y parámetros clínicos para mejorar tanto la precisión diagnóstica como la predicción pronóstica.
Los autores concluyen que la IA no está destinada a reemplazar las modalidades de imagen existentes ni el juicio clínico, sino a complementarlos mediante análisis cuantitativos reproducibles e integrados al flujo de trabajo. La transición desde estudios experimentales hacia una implementación clínica segura y equitativa dependerá de avances en calidad de datos, transparencia algorítmica, regulación y validación en entornos reales.