Investigadores de Johns Hopkins Medicine desarrollaron un modelo de aprendizaje automático para calcular el éxito de la quimioterapia en pacientes con osteosarcoma.
Un equipo de investigación de Johns Hopkins Medicine desarrolló un modelo de aprendizaje automático para calcular el porcentaje de necrosis en pacientes con osteosarcoma, un tipo de cáncer óseo. El modelo logró una precisión del 85% en comparación con los resultados de un patólogo musculoesquelético, y tras eliminar un valor atípico, la precisión se elevó al 99%.
Cabe mencionar que el cálculo de porcentaje de necrosis después de la quimioterapia es importante para proporcionar un pronóstico de supervivencia al paciente. Un porcentaje del 99% indica que el 99% del tumor está muerto, lo que significa que la quimioterapia fue efectiva y que el paciente tiene mejores probabilidades de sobrevivir. Por su parte, los patólogos calculan esta variable mediante la observación y la anotación de imágenes de láminas completas, que son secciones finamente cortadas de una muestra de tejido óseo, montadas en láminas para su análisis microscópico.
Calcular este porcentaje es un proceso tardado y que no solo requiere mucho trabajo sino también una gran cantidad de datos de anotación del patólogo musculoesquelético y, además, tiene una baja fiabilidad entre observadores, lo que significa que dos patólogos que intentan calcularlo a partir de las mismas imágenes de láminas a suelen informar conclusiones diferentes. Por ello, el equipo decidió desarrollar un modelo de aprendizaje automático “débilmente supervisado”, que requería una cantidad mínima de datos de anotación para su entrenamiento. Esto con el propósito de reducir la carga de trabajo del patólogo musculoesquelético que utiliza el modelo.
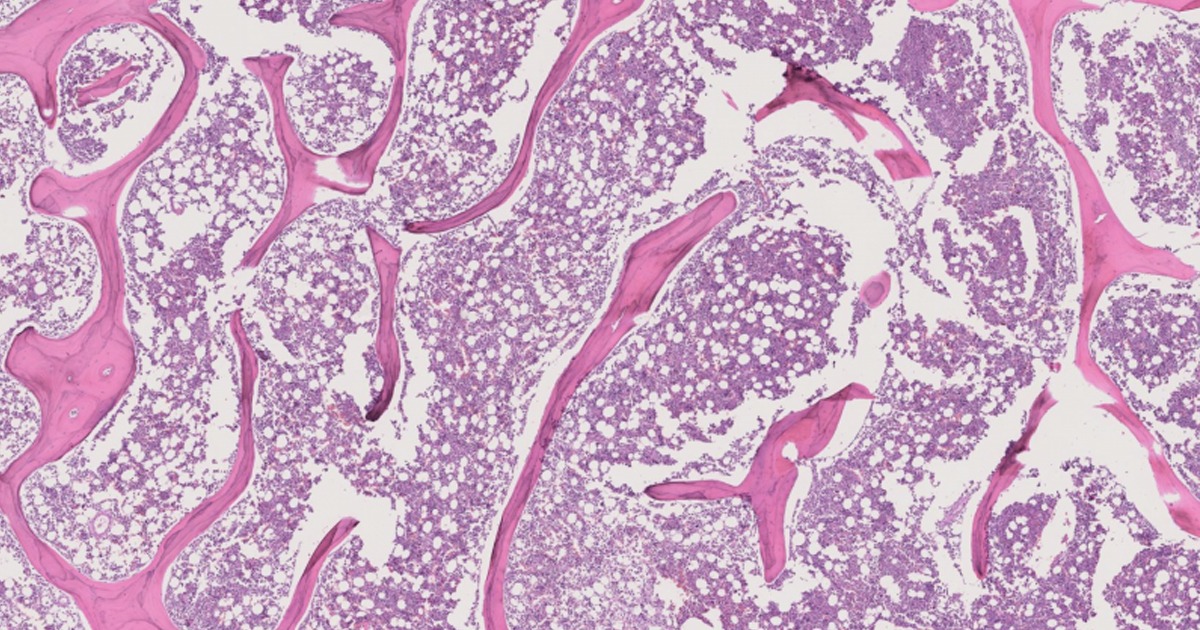
Para entrenar el modelo, el equipo recopiló datos, incluidas imágenes de láminas, de los archivos de patología del centro oncológico terciario de Johns Hopkins. Los datos provenían de pacientes con osteosarcoma intramedular que se sometieron a quimioterapia y cirugía entre 2011 y 2021. Un patólogo musculoesquelético anotó parcialmente tres tipos de tejido en cada una de las imágenes de láminas recopiladas y estimó el porcentaje de necrosis para cada paciente. Con esta información, el equipo comenzó a entrenar el modelo.
“Dividimos las imágenes de láminas en miles de pequeños fragmentos y luego dividimos los fragmentos en grupos en función de cómo los etiquetó el patólogo. Finalmente, alimentamos estos grupos de fragmentos al modelo para entrenarlo. Pensamos que esto le daría al modelo un marco de referencia más sólido que simplemente alimentarlo con una sola imagen de lámina grande y arriesgarse a perder el panorama general”, explicó dice Zhenzhen Wang, coautora del estudio y estudiante de doctorado en ingeniería biomédica en Johns Hopkins.
Tras el entrenamiento, el modelo y el patólogo musculoesquelético interpretaron seis imágenes de láminas de dos pacientes con osteosarcoma. Los resultados mostraron una correlación positiva del 85% entre el modelo y el patólogo en los cálculos de porcentaje de necrosis y etiquetado de tejido. Sin embargo, el modelo no etiquetó adecuadamente el cartílago en una de las imágenes, lo que condujo a un valor atípico. Cuando se excluyó el valor atípico, la correlación aumentó al 99%.
Este modelo tiene el potencial de agilizar la evaluación de la efectividad de la quimioterapia en los pacientes, proporcionando estimaciones de pronóstico más rápidas y reduciendo los costos de atención médica. “Si este modelo se valida y se produce, podría ayudar a acelerar la evaluación de la efectividad de la quimioterapia en un paciente y, por lo tanto, proporcionarle una estimación del pronóstico más pronto”, expresó Christa LiBrizzi, coautora del estudio y residente del Departamento de Cirugía Ortopédica en Johns Hopkins. Además, mencionó que además de reducir los costos de la atención médica, también disminuiría la carga de trabajo de los patólogos musculoesqueléticos.
Consulta el estudio completo en el siguiente enlace: