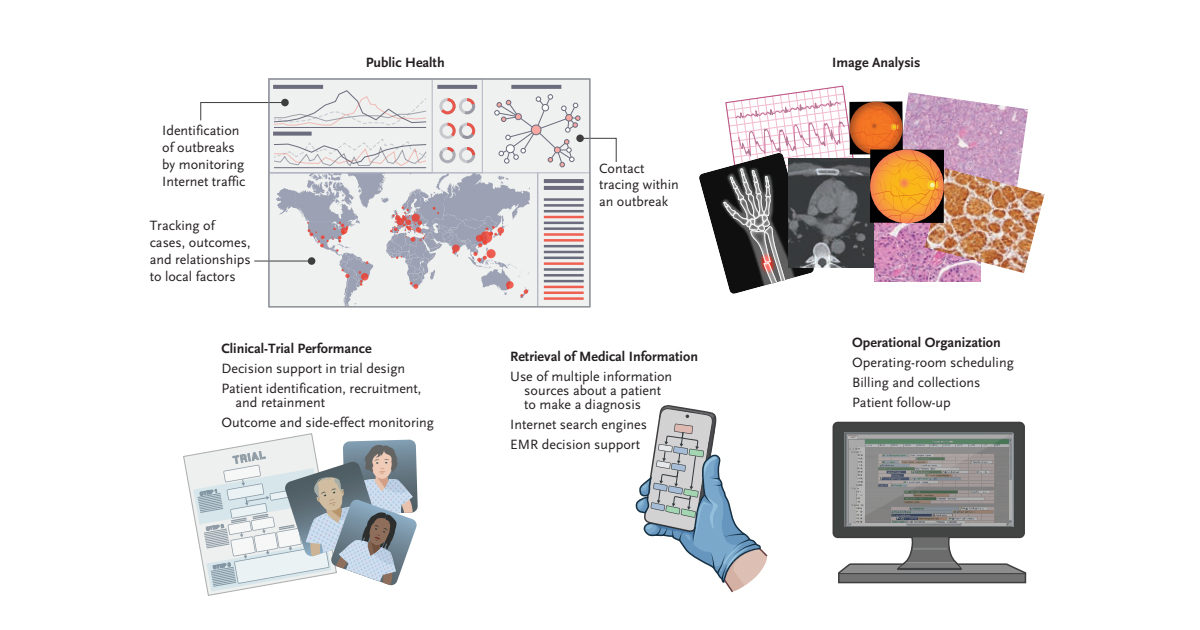
Cofepris estableció un nuevo plan de trabajo para las Unidades de Intercambiabilidad con el fin de fomentar la investigación clínica.
La Comisión Federal para la Protección contra Riesgos Sanitarios (Cofepris) ha anunciado un plan de acción destinado a fortalecer el ecosistema de Unidades de Intercambiabilidad en México, con el objetivo de garantizar el acceso a medicamentos genéricos y biosimilares seguros y eficaces en el país. Este plan incluye medidas para optimizar la evaluación de los protocolos de intercambiabilidad y estudios de bioequivalencia, así como soluciones para evitar prevenciones recurrentes.
En una reciente mesa de trabajo con las Unidades de Bioequivalencia, se identificaron áreas de mejora operativa y regulatoria, lo que condujo al desarrollo de esta estrategia de alineación de criterios. En este sentido, las autoridades prevén la implementación de ajustes en la plataforma Digipris: Investigación y Ensayos Clínicos, con secciones específicas para este tipo de investigaciones, con el fin de ampliar el acceso a medicamentos genéricos y biosimilares seguros y de calidad.
Además, se emitirán nuevos lineamientos para establecer los requisitos para el reconocimiento y la selección de los medicamentos de referencia, permitiendo el uso de fármacos de referencia reconocidos a nivel internacional en protocolos autorizados por Cofepris. De esta manera, la transparencia en los dictámenes sanitarios también será una prioridad, con la publicación de guías que contienen formatos de preevaluación y autoverificación, así como una guía para la obtención y prórroga de la licencia de Unidad de Bioequivalencia.

Cofepris propone un diálogo estrecho y colaborativo con las autoridades y las industrias involucradas para establecer reglas y lineamientos que aborden los futuros desafíos de la investigación clínica. Asimismo, implementarán programas de educación continua en colaboración con centros de investigación y universidades, con el objetivo de fortalecer la capacidad de verificación del personal de Cofepris y mejorar la emisión de dictámenes sanitarios.